Physique – Chimie
Les protides
Les protides sont des composés organiques azotés de la matière vivante comprenant au moins :
- une fonction amine -NH2
- une fonction acide carboxylique -COOH
1. Les acides aminés
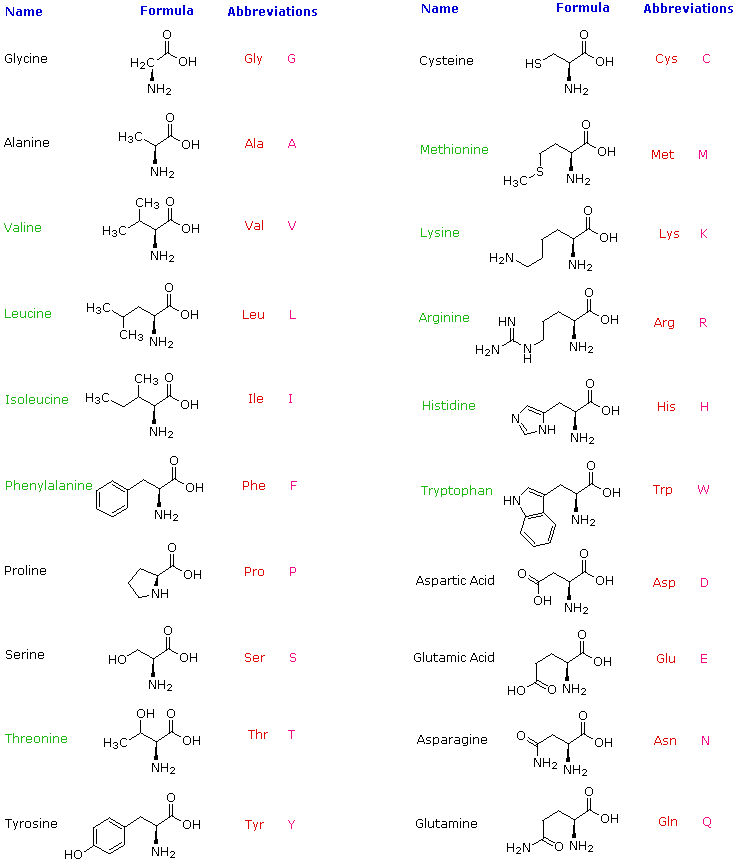
Les protéines sont formées à partir d’un répertoire de 20 acides aminés qui sont donc l’élément de base des protéines.
Un acide aminé est constitué d’une fonction amine, d’un groupe carboxylique, d’un atome d’hydrogène et d’un groupe variable : R. Les chaînes latérales se différencient par leur dimension, leur forme, leur charge, leur capacité à contracter des liaisons hydrogène et leur réactivité chimique.
Les acides α-aminés ont la fonction amine située sur le carbone immédiatement voisin du carbone du groupe carboxyle.
En solution à pH neutre, les acides aminés se trouvent essentiellement sous forme d’ions dipolaires.
Les acides aminés jouent le rôle de régulateur de pH en réagissant comme des acides ou des bases selon le pH de la solution, ils sont amphotères.
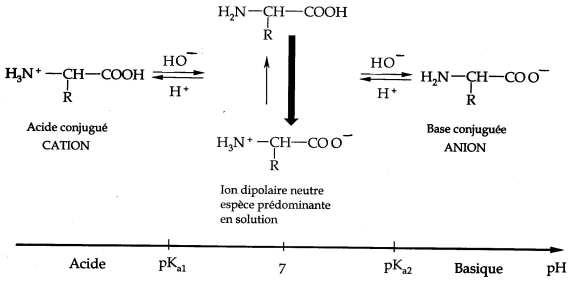
En milieu basique (présence de HO–), la fonction acide est dissociée, neutralisée. En milieu acide (présence de H3O+), la fonction amine est salifiée (Formation d’un sel par réaction d’un acide sur une base).
2. PROTEINES ET PEPTIDES
2.1. LA LIAISON PEPTIDIQUE
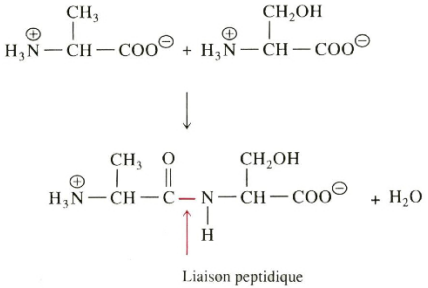
Les protéines et peptides résultent de la condensation d’un grand nombre d’aminoacides.
Dans les protéines, le groupe α carbonyle d’un acide aminé est uni à la fonction amine d’un autre acide aminé par une liaison peptidique. L’extrémité aminée est prise comme origine de la chaîne polypeptidique.
La liaison peptidique possède un caractère de double liaison, ce qui implique que tous les atomes (Cα, C, O, N, H et Cα) soient coplanaires. L’unité peptidique est donc rigide et plane. Par contre la liaison entre l’atome de carbone α et l’atome de carbone du groupement carboxyle est une simple liaison de même que la liaison entre le carbone α et l’atome d’azote peptidique. Il y a un grand degré de liberté de rotation autour de ces liaisons de chaque côté de l’unité peptidique rigide.
2.2. TEST DE LA LIAISON PEPTIDIQUE : la réaction du biuret
Elle caractérise les peptides et protéines contenant au moins 3 acides aminés. En milieu alcalin (NaOH), les liaisons peptidiques forment avec les ions cuivre II (quelques gouttes de sulfate de cuivre) un complexe violet.
Protocole à suivre pour réaliser le test : A une solution peptidique, ajouter de l’hydroxyde de sodium (Na+, OH–) à 0,1 M et du sulfate de cuivre (Cu2+, SO42-). Le test est positif lorsqu’une couleur violette (ou rose) apparait.
