Physique – Chimie
Fiche méthode en laboratoire
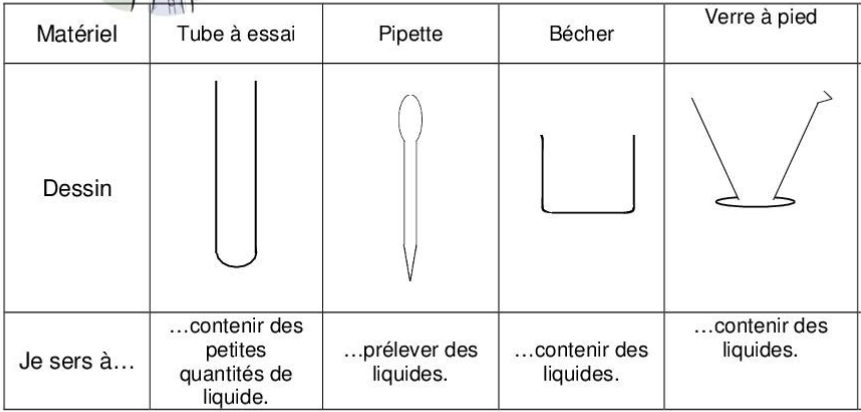
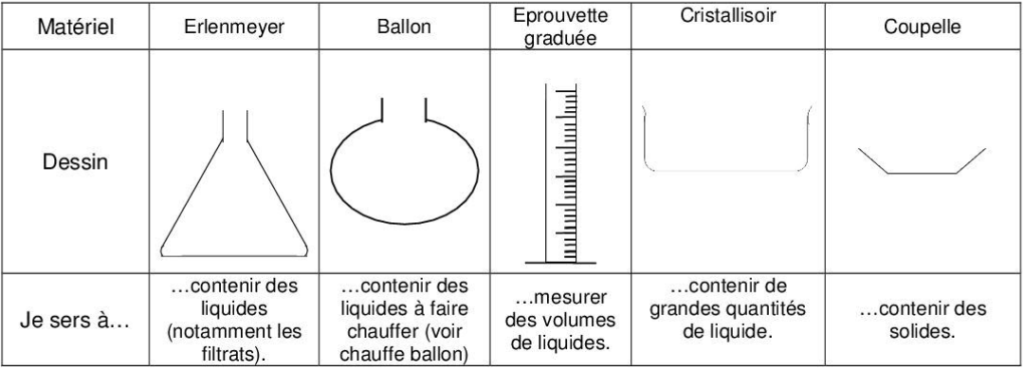
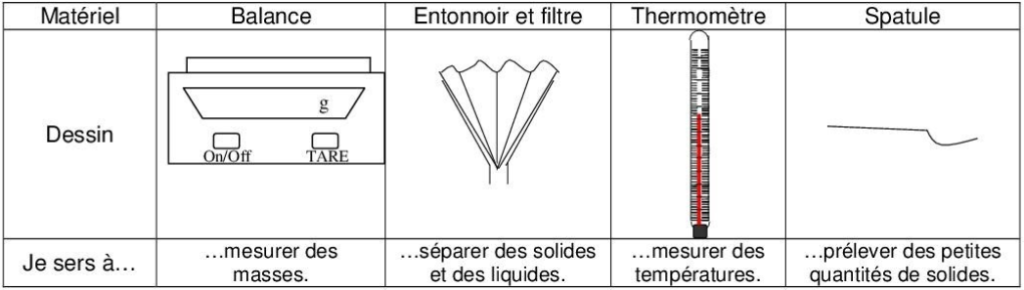
1. Liste de la verrerie de laboratoire
2. Préparation d’une solution par dissolution
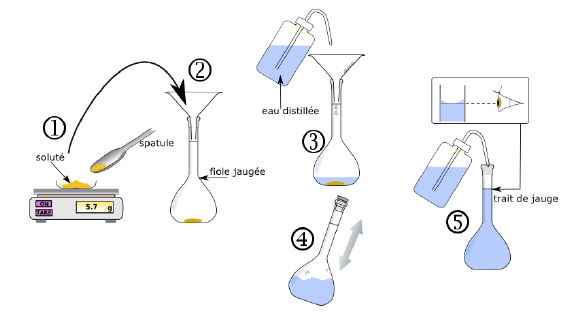
❶ On place une coupelle (ou un verre de montre) sur une balance préalablement tarée puis on pèse précisément la masse m de soluté à dissoudre (masse qu’il aura fallu déterminer au préalable) à l’aide d’une spatule.
❷ On verse le soluté dans une fiole jaugée de volume V à l’aide d’un entonnoir.
❸ On ajoute de l’eau déminéralisée en rinçant les parois de l’entonnoir jusqu’aux ¾. On bouche et on agite pour homogénéiser la solution.
❹ On complète jusqu’au trait de jauge (à l’aide éventuellement d’une pipette Pasteur). On bouche et on agite. (Attention à bien placer son œil : la surface du solvant doit être tangente au bas du ménisque.)
3. Préparation d’une solution par dilution
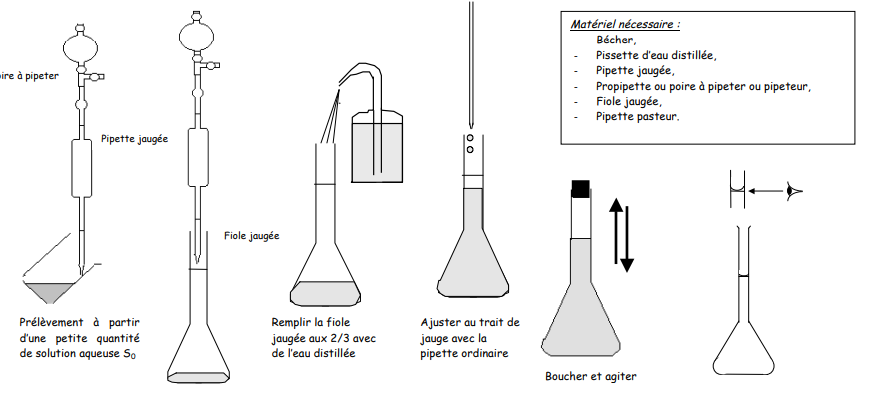
Le but de cette opération est de préparer à partir d’une solution mère S0 (concentration C0) une nouvelle solution fille S moins concentrée (concentration C).
Lors d’une dilution, il y a conservation de la quantité de matière de l’espèce dissoute. La quantité de matière : n = C0.V0 = C.V
avec V = volume final de la solution fille (volume de la fiole jaugée).
et V0 = volume à prélever de la solution mère (volume de la pipette jaugée) : V0 = C.V / C0
S’il faut diluer la solution mère 10 fois (F =10), on définit le facteur de dilution F comme le rapport : F = C0/C = V/V0
C0/C = 10 ⇔ V0 = V/F = V/10
